LA TABLA PERIODICA. LOS ENLACES
LA TABLA PERIODICA
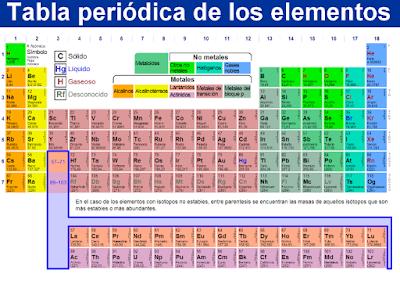
De esa manera, los elementos que se comportan de manera semejante ocupan renglones cercanos, y se identifican en grupos (columnas, dieciocho en total) y períodos (filas, siete en total). En principio, toda la materia conocida del universo está compuesta por diversas combinaciones de los elementos que se encuentran en esta tabla: hasta ahora se conocen 118 elementos.
Los elementos de la Tabla Periódica, además, están representados con sus respectivos símbolos químicos, y a través de un sistema de colores que indica el estado de agregación del elemento a una temperatura de 0 °C y una presión de 1 atmósfera: rojo (gaseoso), azul (líquido), negro (sólido) y gris (desconocido).
La Tabla Periódica es una herramienta fundamental para la química, la biología y otras ciencias naturales, que se actualiza con el pasar de los años, conforme aprendemos más sobre los patrones de la materia y las relaciones entre los elementos.
Fuente: https://concepto.de/tabla-periodica/#ixzz6Hg50V6CC
¿QUÉ ES LA TABLA PERIODICA?
Se denomina Tabla Periódica de los Elementos o simplemente Tabla
Periódica a una herramienta gráfica en la que figuran todos los elementos químicos
conocidos por la humanidad, organizados conforme al número de protones de sus átomos, también llamado número atómico, y tomando
en cuenta también la configuración de sus electrones y las propiedades químicas
específicas que presentan.Bloques de la tabla periódica
La tabla periódica se puede también dividir en bloques de elementos
según el orbital que estén ocupando los electrones más externos.
Los bloques o regiones se denominan según la letra que hace referencia al orbital más externo: s, p, d y f. Podría haber más elementos que llenarían otros orbitales, pero no se han sintetizado o descubierto; en este caso se continúa con el orden alfabético para nombrarlos.
Bloque s
Los bloques o regiones se denominan según la letra que hace referencia al orbital más externo: s, p, d y f. Podría haber más elementos que llenarían otros orbitales, pero no se han sintetizado o descubierto; en este caso se continúa con el orden alfabético para nombrarlos.
Los elementos del bloque s (por tener sus electrones de
valencia en el orbital s) son aquellos situados en los grupos 1 y 2 de la tabla
periódica de los elementos. En estos elementos el nivel energético más externo
corresponde a orbitales s
Bloque p
Los elementos del bloque p (por tener sus electrones de
valencia en el orbital p) son aquellos situados en los grupos 13 a 18 de la
tabla periódica de los elementos. En estos elementos el nivel energético más
externo corresponde a orbitales p. La configuración electrónica externa de
estos elementos es: ns²npx (x=1 a 6, siendo 1 para el primer grupo, 2 para el
segundo, etc.)
Bloque d
Los elementos del bloque d (por tener electrones en el
orbital d) son aquellos situados en los grupos 3 a 12 de la tabla periódica de
los elementos. En estos elementos el nivel energético más externo corresponde a
orbitales d.
Bloque f
Bloque f
Los elementos del bloque f (por tener sus
electrones de valencia en el orbital f) son dos series, una comenzando a partir
del elemento lantano y la otra a partir del actinio, y por eso a los elementos
de estas series se les llama lantánidos y actínidos. Aunque en la tabla periódica
de los elementos tendrían que estar después de esos dos elementos, se suelen
representar separados del resto. También se conocen los Lantánidos como tierras
raras.
De esa manera, los elementos que se comportan de manera semejante ocupan renglones cercanos, y se identifican en grupos (columnas, dieciocho en total) y períodos (filas, siete en total). En principio, toda la materia conocida del universo está compuesta por diversas combinaciones de los elementos que se encuentran en esta tabla: hasta ahora se conocen 118 elementos.
Los elementos de la Tabla Periódica, además, están representados con sus respectivos símbolos químicos, y a través de un sistema de colores que indica el estado de agregación del elemento a una temperatura de 0 °C y una presión de 1 atmósfera: rojo (gaseoso), azul (líquido), negro (sólido) y gris (desconocido).
La Tabla Periódica es una herramienta fundamental para la química, la biología y otras ciencias naturales, que se actualiza con el pasar de los años, conforme aprendemos más sobre los patrones de la materia y las relaciones entre los elementos.
Fuente: https://concepto.de/tabla-periodica/#ixzz6Hg50V6CC
El sistema periódico actual se
basa en la ordenación de los elementos químicos según orden creciente de
números atómicos, ya que se ha mostrado que las propiedades químicas, y algunas
propiedades físicas, dependen de la configuración electrónica de la última capa
de los átomos.
LOS PERIODOS Y GRUPOS
LOS PERIODOS
Los Períodos o Familias son las filas horizontales de la Tabla Periódica .
Los Períodos representan los niveles energéticos que tiene un átomo. Así, como el hierro (Fe) tiene cuatro niveles energéticos, pertenece por lo tanto al cuarto período.
Los Períodos representan los niveles energéticos que tiene un átomo. Así, como el hierro (Fe) tiene cuatro niveles energéticos, pertenece por lo tanto al cuarto período.
La Tabla Periódica consta de 7 períodos:
- Período 1
- Período 2
- Período 3
- Período 4
- Período 5
- Período 6
- Período 7
-
Con el nombre de período, la Química distingue cada una de las siete líneas
horizontales, mostradas de arriba a abajo, que componen la Tabla Periódica.
También están numeradas del 1 al 7, lo que no sólo es así en su orden
correlativo, sino también porque el número de cada uno de los períodos indica
el número del nivel de energía principal que los electrones de los elementos,
pertenecientes a un período específico, comienzan a llenar. Según la
distribución actual y la conformación de este cuadro de clasificación química,
se pueden encontrar siete tipos diferentes de períodos.
LOS GRUPOS
EVALUACION -
LEA CON ATENCIÓN EN EL TEXTO Y PONGA LOS SÍMBOLOS DE CADA ELEMENTO EN EL GRUPO O FAMILIA AL QUE PERTENECE EN EL TEXTO PAGINAS 51 Y 52



Comentarios
Publicar un comentario