LOS ENLACES: TIPOS DE ENLACES
TIPOS DE ENLACES
• Compuestos iónicos
• Compuestos covalentes
• Fuerzas de atracción intermolecular
• Enlace metálico
• Clases de enlaces
• Compuestos iónicos
• Compuestos covalentes
• Fuerzas de atracción intermolecular
• Enlace metálico
INFORMACIÓN DEL
CONOCIMIENTO:
• CLASES
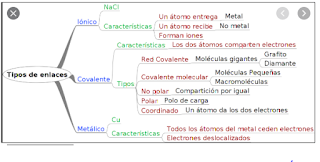
DE ENLACES: Los átomos se unen entre sí para formar moléculas mediante
fuerzas de enlace. Los tipos
fundamentales de enlace son el
iónico, el covalente y el metálico,
Compuestos
iónicos
Son compuestos iónicos, en general:
• Las sales binarias (NaCl, CaF2…).
• Las sales ternarias (KClO3, CaSO4…).
• Algunos óxidos (Li2O, CaO…).
• Algunos hidróxidos (NaOH, KOH…).
Observa en todos ellos la presencia de elementos de gran carácter metálico junto a elementos electronegativos
Son compuestos iónicos, en general:
• Las sales binarias (NaCl, CaF2…).
• Las sales ternarias (KClO3, CaSO4…).
• Algunos óxidos (Li2O, CaO…).
• Algunos hidróxidos (NaOH, KOH…).
Observa en todos ellos la presencia de elementos de gran carácter metálico junto a elementos electronegativos
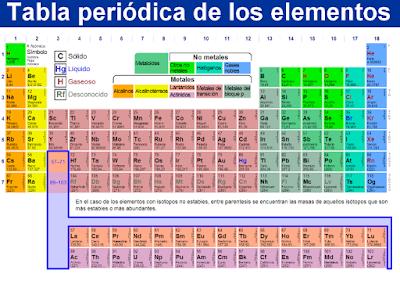
Los elementos metálicos,
situados a la izquierda y en el centro de la tabla periódica, tienden a perder electrones para formar iones positivos o cationes.
Los elementos no metálicos, situados a la derecha de la tabla periódica, tienden a ganar electrones para formar iones negativos o aniones.
Este tipo de enlace se produce cuando se combinan los metales con los no metales.
Los elementos no metálicos, situados a la derecha de la tabla periódica, tienden a ganar electrones para formar iones negativos o aniones.
Este tipo de enlace se produce cuando se combinan los metales con los no metales.
Los iones formados, al tener cargas opuestas, se atraen y permanecen
unidos por fuerzas de atracción
electrostáticas.
Cuando un número muy elevado de cationes interacciona con un número muy elevado de aniones, el conjunto adquiere estabilidad y se forma una red cristalina iónica o cristal iónico
Cuando un número muy elevado de cationes interacciona con un número muy elevado de aniones, el conjunto adquiere estabilidad y se forma una red cristalina iónica o cristal iónico
Propiedades de las
sustancias iónicas
Las sustancias iónicas pueden tener las siguientes propiedades:
• A temperatura ambiente son sólidos de elevado punto de fusión.
• Son solubles en agua.
• En disoluciones acuosas o fundidas conducen corriente eléctrica, pero no en estado sólido.
Las sustancias iónicas pueden tener las siguientes propiedades:
• A temperatura ambiente son sólidos de elevado punto de fusión.
• Son solubles en agua.
• En disoluciones acuosas o fundidas conducen corriente eléctrica, pero no en estado sólido.
ACTIVIDADES:
1- MIRE EL VIDEO DEL SIGUIENTE LINK
https://www.youtube.com/watch?v=hd1eTxqozSs
1- MIRE EL VIDEO DEL SIGUIENTE LINK
https://www.youtube.com/watch?v=hd1eTxqozSs
1.
ESCRIBA
4 EJEMPLOS DE ENLACES IONICOS
2.
EXPLICA LA FORMACIÓN DE LOS SIGUIENTES ENLACES IÓNICOS, UTILIZA LA ESTRUCTURA PUNTUAL DE LEWIS:
A ) EL Na( Z=11) CON
EL Cl ( Z=17 )
B ) El
Mg( Z=12) con el F ( Z=9





Comentarios
Publicar un comentario