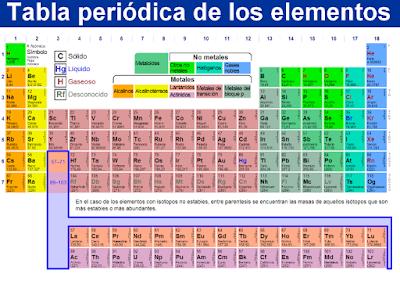
La Tabla Períodica: propiedades períodicas
DÉCIMO
PRIMERO PLAN DE CLASE DE QUIMICA SEGUNDO-PARCIAL
SEGUNDO QUIMESTRE
(CONTINGENCIA COVID19)
1.
DATOS
INFORMATIVOS:
Docente: Lic. Rocío Bayas V.
Área: Ciencias Naturales
Curso:
Primeros A, B, C
Unidad:
Cuatro Fecha: 25/05/2020- 29-05-2020
Tema: La tabla periódica propiedades periodicas
Energía de ionización
y
afinidad electrónica
• Electronegatividad y
carácter metálico
afinidad electrónica
• Electronegatividad y
carácter metálico
se forma covalente polar, con el átomo más electronegativo
quedándose con la carga negativa
EL RADIO ATOMICO. Identifica la distancia que existe
entre el núcleo, y el orbital más externo de un átomo. Por medio del radio
atómico, es posible determinar el tamaño del átomo. En los
grupos, el radio atómico aumenta con el número atómico, es decir
hacia abajo.
¿Por qué
el radio atómico es una propiedad periódica de los elementos
Por que el radio atómico te permite conocer la distancia media que existe
entre los núcleos atómicos de dos átomos que se encuentren unidos mediante un enlace,
y estos atomos o elementos se encuentran dentro de la tabla periodica.
RADIO IONICO El radio iónico es el radio que tiene
un átomo cuando ha perdido o ganado electrones, adquiriendo la estructura
electrónica del gas noble más cercano.
AFINIDAD ELECTRÓNICA
La
afinidad electrónica o electroafinidad se define como la energía liberada
cuando un átomo gaseoso neutro en su estado fundamental captura un electrón y
forma un ion mononegativo
La afinidad electrónica es la
cantidad de energía absorbida por un átomo aislado
en fase gaseosa para
formar un ión con una carga eléctrica de -1. Si la energía no es
absorbida, sino liberada en el proceso, la afinidad electrónica tendrá, en
consecuencia, valor negativo tal y como sucede para la mayoría de los elementos químicos; en la medida en que la
tendencia a adquirir electrones adicionales
sea mayor, tanto más negativa será la afinidad electrónica. De este modo,
el flúor es
el elemento que con mayor facilidad adquiere un electrón adicional, mientras
que el mercurio es el que menos.
|
EVALUACIÓN
:
Copiar el resumen de
los temas tratados en el bloque 2. Pagina 64
Copiar el organizador
gráfico de “usos y aplicaciones de las tierras
raras”
Pagina
58
|
||
|
BIBLIOGRAFIA: Texto de química del ministerio
|
||
|
OBSERVACIONES: Este
tema está planificado para la semana del 25
al 29 de mayo
Todas
las actividades serán incluidas por
semanas en el portafolio que será entregado a la tutora en julio
|
||
|
FIRMAS
|
||
|
ELABORADO POR:
|
REVISADO POR
|
AVALADO POR
|
|
Lic. Rocío BayasV.
DOCENTE-QUIMICA
|
Msc. Ligia Rojas C.
JEFE
DE ÁREA
|
Ing.
Miguel Sánchez
VICERRECTOR
(E)
|





Comentarios
Publicar un comentario